메드트로닉은 지난 2일 제 4차 ‘아뉴렉스 임상 업데이트(AneuRx Clinical Update)’ 결과를 발표했다.
이는 상용화된 혈관이식편 제품(endograft) 관련 임상데이터 중 가장 규모가 크며, 1996년부터 사용된 제품 70,000개와 1,000명의 환자를 대상으로 한 것이다.
이 자료는 학술지인 ‘Endovascular Today’ 2007년 9월호에 실렸으며, 전세계 18,000명의 의사들에게 배포, 인터넷www.medtronic.com/physician/AneuRx에서도 열람이 가능하다.
관련 분야에서 10년 이상의 경력을 보유한 하버-UCLA 메디컬 센터의 로드니 화이트 박사(Dr. Rodney White, Harbor-UCLA Medical Center)는 “이 보고서는 혈관 수술의사에게 아뉴렉스 스텐트 그래프트(AneuRx Stent Graft)의 장기간 안전성과 효능과 관련하여 깊이 있는 분석을 제공한다. 지속적으로 환자 결과와 제품 성능을 연구조사해온 메드트로닉의 공로를 높이 산다”고 말했다.
이번 자료는 ‘AneuRx IDE’ 임상연구(AneuRx IDE Clinical Trial)의 장기 추적관찰 데이터의 최신 자료를 기반으로 하고 있다. ‘AneuRx IDE’ 임상연구는 AneuRx 초기 모델로 치료받은 1,193명의 환자를 대상으로 하였다. 환자 600명을 수술 5년 후 추적 관찰한 결과, 96%에서 동맥류(aneurysm)관련 사망이 발생하지 않았으며, 좀더 포괄적인 FDA 정의를 사용하여 동맥류 관련 사망을 분석한 결과, 수술 5년 후 94.6%에서 동맥류 관련 사망이 발생하지 않았다. 4년에서 5년 사이 추적 관찰 사이에 동맥류 관련 사망 증가가 관찰되었으나, 후기 동맥류관련 사망이 발생한 것은 추적관찰 미비, 치료 거부 그리고 고령의 환자군 등이었다.
개정된 IDE 임상연구 결과뿐만 아니라, 메드트로닉은 또한 아뉴렉스 스텐트 그래프트(AneuRx Stent Graft)에 대한 현재 실세계(real-world) 사용 데이터를 제공하는 ‘AneuRx Post-Market Surveillance Registry’와 ‘the Lifeline Registry of Endovascular Aneurysm Repair’에 대해서도 보고하였다.
‘Post-Market Surveillance Registry’에 의하면 수술 3년 후 환자 99%에서 동맥류 파열이 일어나지 않았고, 96%에서 수술로 전환(surgical conversion)되지 않았다. 이들 두 데이터에서 제품 이식 부위로부터 위치 이동은 334명의 환자군에서 단 한 건이었으며, 이도 수술 3년 후 0.3%의 위치이동이었다.
임상 업데이트에서는 혈관누출(endoleaks), 위치 이동 그리고 적절한 환자 추적관찰의 중요성 등을 중요하게 다루고 있다. 말초혈관(Endovascular) 동맥류 치유에 사용되는 다른 제품들과 마찬가지로, 환자의 추적관찰 순응도(patient follow-up compliance)는 성공적인 장기 결과에 매우 중요하다.
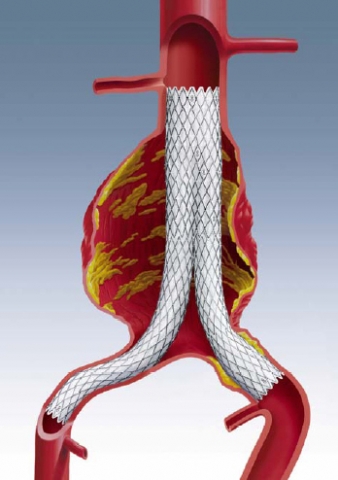
메드트로닉은 최신의 혁신 제품인 ‘AneuRx AAAdvantage Stent Graft system’으로 복부대동맥류(AAA, Abdominal Aortic Aneurysm) 치료에서 선두를 유지하고 있으며, 차세대 제품에는 더 사용하기 쉽고, 환자에 적용하기 쉬우며 스텐트 그래프트 전달(delivery)이 더 정확하게 할 수 있는 테크놀로지를 적용할 계획이다.
메드트로닉 말초혈관사업부 부사장인 케이티 시먼(Katie Szyman)은 “메드트로닉은 지난 11년간 복부대동맥류 치료법을 향상시키고 환자 결과를 극대화하기 위해, 제품 사용 테크닉, 적절한 환자선택 그리고 테크놀로지 개선에 있어 우리와 함께 노력해주신 임상연구가들과 의사들에게 감사를 드린다. 우리는 혈관이식편 제품의 성능을 지속적으로 연구조사하고 최신의 임상 데이터와 정보를 의사에게 제공하여 환자 치료를 극대화할 수 있도록 노력할 것이다.”라고 말했다.
혈관이식편(endograft)은 스텐트와 비슷한 의료기기로 치명적인 ‘복부 대동맥류(AAA, Abdominal Aortic Aneurysms)’치료에 사용된다. 혈관이식편 대신 외과 수술을 할 수 있으나, 이 경우 수술 30일 후 사망률이 3~5%이다.
메드트로닉코리아 개요
메드트로닉은 미국 미네소타 주 미니애폴리스에 본사를 두고 있는 전세계적인 의료기기 선두기업으로 전세계 수백만명의 "고통을 덜어주고, 건강을 회복시키고, 생명을 연장시킨다-Alleviating Pain, Restoring Health, Extending Life"는 사명을 가지고 있다.
웹사이트: http://www.medtronic.co.kr
연락처
메드트로닉코리아 홍보팀 이연숙 대리, 02-3404-3154, 이메일 보내기